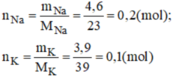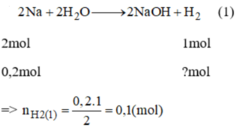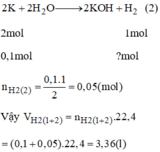Cho một hỗn hợp chứa 2,3 g natri và 7,8 g kali tác dụng hết với nước .thể tích khí H2 thu được ở đktc là :

Những câu hỏi liên quan
Có một hỗn hợp chứa 2,3 gam natri và 1,95 gam kali tác dụng với nước. Thể tích khí hiđro thu được (đktc) là *
\(2Na+2H_2O\rightarrow2NaOH+H_2\\2K+2H_2O\rightarrow2KOH+H_2\\ n_{Na}=0,1\left(mol\right);n_K=0,05\left(mol\right)\\ n_{H_2}=\dfrac{1}{2}n_{Na}+\dfrac{1}{2}n_K=0,05+0,025=0,075\left(mol\right)\\ \Rightarrow V_{H_2}=0,075.22,4=1,68\left(l\right)\)
Đúng 0
Bình luận (0)
Cho một hỗn hợp chứa 4,6g natri và 3,9g kali tác dụng với nước. Tính thể tích khí hidro thu được (đktc)
3. Cho một hỗn hợp chứa 4,6g natri và 3,9g kali tác dụng với nước.
a) Viết phương trình phản ứng xảy ra
b) Tính thể tích khí hidro thu được (ở đktc)
c) Tính nồng độ phần trăm của dung dịch sau phản ứng biết khối lượng nước là 91,5g
giúp mk vs ạ mk cần gấp
a,\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,2 0,1
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 0,1 0,05
b, \(n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,mdd sau pứ=4,6+3,9+91,5-0,15.2=99,7 (g)
\(\%m_{NaOH}=\dfrac{0,2.40.100\%}{99,7}=8,02\%\)
\(\%m_{KOH}=\dfrac{0,1.56.100\%}{99,7}=5,62\%\)
Đúng 1
Bình luận (0)
Bài 3 :
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
a) Pt : \(2Na+2H_2O\rightarrow2NaOH+H_2|\)
2 2 2 1
0,2 0,2 0,1
\(2K+2H_2O\rightarrow2KOH+H_2|\)
2 2 2 1
0,1 0,1 0,05
b) \(n_{H2\left(tổng\right)}=0,1+0,05=0,15\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.22,4=3,36\left(l\right)\)
c) \(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(n_{KOH}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
⇒ \(m_{KOH}=0,1.56=5,6\left(g\right)\)
\(m_{ddspu}=8,5+91,5-\left(0,15.2\right)=99,7\left(g\right)\)
\(C_{NaOH}=\dfrac{8.100}{99,7}=8,02\)0/0
\(C_{KOH}=\dfrac{5,6.100}{99,7}=5,62\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho hỗn hợp chứa 4,6 gam natri và 3,9 gam Kali tác dụng với nước: A.viết phương trình phản ứng B.tính thể tích khí hiđro thu được (đktc)
Em đang cần câi này gấp để chiều thi ai giúp em với
Đúng 0
Bình luận (0)
\(a,PTHH:2Na+2H_2O\rightarrow2NaOH+H_2\\ 2K+2H_2O\rightarrow2KOH+H_2\\ n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right);n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\\ b,n_{H_2\left(tổng\right)}=\dfrac{1}{2}.\left(n_{Na}+n_K\right)=\dfrac{0,2+0,1}{2}=0,15\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
cho 1 hỗn hợp chứa 4,6 g Natri và 3,9 gam Kali tác dụng với H2O
a).Viết phương trình phản ứng
b).tính thể tích khí hidro thu được ở điều kiện tiêu chuẩn
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(n_K=\dfrac{3.9}{39}=0.1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(n_{H_2}=0.1+0.05=0.15\left(mol\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
Đúng 2
Bình luận (1)
a) nNa=4,6/23=0,2(mol)
nK=3,9/39=0,1(mol)
PTHH: 2 Na + 2 H2O -> 2 NaOH + H2
0,2____________0,2______0,2__0,1(mol)
2 K + 2 H2O -> 2 KOH + H2
0,1____0,1______0,1___0,05(mol)
b) V(H2,đktc)=(0,05+0,1).22,4=3,36(l)
Đúng 2
Bình luận (0)
Cho 1,24 g hỗn hợp Na và K tác dụng hết với nước, sau phản ứng thu được 1,92 gam hỗn hợp 2 bazơ NaOH và KOH. Thể tích khí H 2 sinh ra ở đktc là:
A. 0,224 lít
B. 0,48 lít
C. 0,336 lít
D. 0,448 lít.
Bài 13: Cho một hỗn hợp chứa 4,6 g natri và 3,9 g kali tác dụng với nước .
a) Tính thể tích khí hiđro thu được (đktc ) ?
b) Tính nồng độ phần trăm của dung dịch biết khối lượng nước là 91,5 g?
Bài 14: Ở 20o C, khi hòa tan 60 gam KNO3 vào 190 nước thì thu được dung dịch bão hòa. Tính độ tan của KNO3 ở nhiệt độ đó?
Bài 13: nNa= 0,2 mol ; nK= 0,1 mol
2Na + 2H2O → 2NaOH + H2↑
0,2 mol 0,2 mol 0,1 mol
2K + 2H2O → 2KOH + H2↑
0,1 mol 0,1 mol 0,05 mol
a) tổng số mol khí H2 là: nH2= 0,1 + 0,05 = 0,15 mol
→VH2= 0,15 x 22,4 = 3,36 (l)
b) mNaOH= 0,2 x 40= 8 (g) ; mKOH= 0,1 x 56= 5,6 (g)
mdung dịch= mNa + mK + mH2O - mH2 = 4,6 + 3,9 + 91,5 - 0,15x2 = 99,7 (g)
→C%NaOH= 8/99,7 x100%= 8,02%
→C%KOH= 5,6/99,7 x100%= 5,62%
Đúng 0
Bình luận (3)
Cho một hỗn hợp chứa 4,6 g natri và 3,9 g kali tác dụng vs nước.
a,Viết phương trình hóa học
b,Tính thể tích khí hiđro thu đc
c, Dung dịch sau phản ứng làm đổi màu giấy tùy tím như thế nào?
Xem chi tiết
a) \(2Na+2H_2O\rightarrow2NaOH+H_2\left(1\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\left(2\right)\)
b) \(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
Theo PTHH (1): \(n_{Na}:n_{H_2}=2:1\)
\(\Rightarrow n_{H_2\left(1\right)}=n_{Na}.\frac{1}{2}=0,2.\frac{1}{2}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2\left(1\right)}=0,1.22,4=2,24\left(l\right)\)
\(n_K=\frac{3,9}{39}=0,1\left(mol\right)\)
Theo PTHH (2): \(n_K:n_{H_2}=2:1\)
\(\Rightarrow n_{H_2\left(2\right)}=n_K.\frac{1}{2}=0,1.\frac{1}{2}=0,05\left(mol\right)\)
\(\Rightarrow V_{H_2\left(2\right)}=0,05.22,4=1,12\left(l\right)\)
\(\Rightarrow V_{h^2}=2,24+1,12=3,36\left(l\right)\)
c) Dung dịch thu được sau phản ứng làm giấy quỳ tím chuyển đổi thành màu xanh vì nó là dung dịch bazơ.
Đúng 1
Bình luận (0)
Cho 1,77 g hỗn hợp Ca và Ba tác dụng hết với nước, sau phản ứng thu được 2,45g hỗn hợp 2 bazơ
C
a
O
H
2
và
B
a
O
H
2
. Thể tích khí
H
2
sinh ra ở đktc là: A. 0,224 lít B. 0,448 lít C....
Đọc tiếp
Cho 1,77 g hỗn hợp Ca và Ba tác dụng hết với nước, sau phản ứng thu được 2,45g hỗn hợp 2 bazơ C a O H 2 và B a O H 2 . Thể tích khí H 2 sinh ra ở đktc là:
A. 0,224 lít
B. 0,448 lít
C. 0,336 lít
D. 0,48 lít
Ca + 2 H 2 O → C a O H 2 + H 2
x……...x………x….mol
Ba + 2 H 2 O → B a O H 2 + H 2
y……y……..y……mol
Giải hệ phương trình:
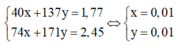
⇒ n H 2 = x+y = 0,02 mol
⇒ V H 2 = 0,02.22,4 = 0,448 lit
⇒ Chọn B.
Đúng 0
Bình luận (0)